Suplementos para el TDAH: lo prometedor, lo útil y lo que no es para tanto
Una mirada de cuerpo entero al azafrán, la corteza de pino, la melatonina, los omega-3, los suplementos dirigidos al intestino, la vitamina D, el magnesio y la L-teanina, para empezar…
Cuando la gente me pregunta si los suplementos ayudan en el TDAH, rara vez empiezo preguntándome si un suplemento “funciona”. Empiezo en otro sitio. Me pregunto qué, exactamente, estamos intentando apoyar. ¿La atención? ¿El sueño? ¿La estabilidad emocional? ¿El apetito? ¿El estado nutricional? ¿Los síntomas digestivos? ¿El desgaste acumulado de vivir en un sistema nervioso que ha tenido que trabajar muchísimo durante muchísimo tiempo? Sería mucho más fácil decir sí o no y luego citar una serie de estudios para alardear de lo mucho que he leído… Pero, como buen TDAHero, prefiero las respuestas más largas. De hecho, mis respuestas favoritas son las que hacen replantearnos lo que cuestionábamos, porque, según mejora la pregunta, suele mejorar la conversación.
Esto importa, y mucho, porque el TDAH no es una sola cosa. No es solo hiperactividad o inatención, así que rara vez tiene sentido abordarlo desde un único ángulo. En mi experiencia, es muy fácil acabar con dos relatos igual de poco útiles. En uno, los suplementos se descartan por completo. Y en el otro, su eficacia se infla hasta convertirse en una especie de redención nutricional, como si la cápsula del suplemento X pudiera sustituir a la medicación, al movimiento, al sueño, a la terapia, a la creatividad, a la comprensión de una misma persona y al andamiaje práctico que tantas veces necesitamos de verdad. Yo no estoy de acuerdo con ninguna de esas dos versiones.
Sí, creo que algunos suplementos merecen ser considerados y que algunos son prometedores. Pero no creo que los suplementos sustituyan a la medicación ni a ninguna otra modalidad terapéutica para el TDAH. La base de evidencia de los estimulantes en adultos sigue siendo mucho más sólida que la de los suplementos cuando hablamos de síntomas nucleares del TDAH, y guías clínicas serias y respetadas mundialmente como NICE (el National Institute for Health and Care Excellence en el Reino Unido) siguen recomendando metilfenidato o lisdexanfetamina como tratamiento farmacológico de primera línea en adultos cuando la medicación está indicada. Al mismo tiempo, el cuidado más amplio sigue importando, y NICE deja claro que el manejo del TDAH no consiste solo en una terapia farmacológica. ¹
¿Qué dice la evidencia sobre azafrán, omega-3, melatonina, probióticos, magnesio y otros apoyos nutricionales?
Lo que suelo hacer cuando leo estudios sobre suplementos no es simplemente preguntarme si el resultado es positivo. Me fijo en cosas como si el estudio se hizo en niños o en adultos, si es un piloto o un ensayo más amplio, idealmente aleatorizado y ciego, o si es un estudio abierto y sin “randomizar”. También me parece importante saber si el suplemento se ha usado como tratamiento único o como complemento, y en qué se basa la hipótesis central del estudio. El TDAH no va solo de dopamina, de foco y de hiperactividad. Un estudio bien diseñado, desde mi punto de vista, debería investigar los efectos del suplemento sobre el sueño, el estado de ánimo, la conducta y el estrés oxidativo, además de los síntomas nucleares del TDAH. Y luego está la demografía. Si el estudio sólo incluye niños y no niñas, o si un estudio solo incluye hombres adultos, siempre será mucho más difícil generalizar las conclusiones a las mujeres. Todos estos detalles importan mucho más de lo que se suele pensar, porque nos dicen hasta dónde puede viajar razonablemente un hallazgo más allá de la muestra original.
Los omega-3
Los omega-3 siguen mereciendo formar parte de la conversación, pero la historia se tiene que abordar con un pelín de sal, como se dice en inglés, es decir, de manera matizada. Los aceites de pescado, o de algas para quienes prefieren no consumir productos animales, son de los suplementos más investigados en TDAH, y esa es una de las razones por las que siguen apareciendo en la conversación. El problema es que a menudo se confunde “de los más investigados” con “claramente eficaz”. La Cochrane Collaboration, una red internacional independiente y sin ánimo de lucro que produce revisiones sistemáticas de alta calidad sobre intervenciones en salud, publicó una actualización en 2023 cuya conclusión fue que, en conjunto, había poca evidencia de que la suplementación con ácidos grasos poliinsaturados mejorara los síntomas del TDAH en niños y adolescentes. ² Un metaanálisis publicado ese mismo año tampoco encontró un efecto global significativo sobre los síntomas nucleares del TDAH, aunque los ensayos más largos, de al menos 4 meses, parecían algo más prometedores. En ese caso, la posible ventaja seguía refiriéndose a los síntomas nucleares del propio TDAH, no a beneficios más generales, por ejemplo cardiovasculares, y además el estudio no permite afirmar con claridad qué dimensión concreta, inatención, hiperactividad o impulsividad, fue la que más se benefició. ³
Dicho esto, no toda la literatura va en la misma dirección. Un metaanálisis anterior, el de Chang et al., sí encontró que la suplementación con omega-3 podía mejorar de forma modesta los síntomas clínicos del TDAH y algunas medidas cognitivas relacionadas con la atención en niños y adolescentes, además de observar que los jóvenes con TDAH tendían a presentar niveles más bajos de DHA, EPA y omega-3 totales que los controles. ⁴ Esto no invalida las revisiones más prudentes, pero sí nos obliga a no caer en mensajes binarios. La lectura más honesta, para mí, es que puede haber una señal real, aunque pequeña, especialmente en población infantojuvenil y quizá en intervenciones más prolongadas, sin que eso justifique presentar los omega-3 como una intervención contundente ni extrapolar sin más esos resultados a adultos.
Omega-3: Veredicto
Para mí, los omega-3 siguen teniendo sentido como apoyo de base, con plausibilidad antiinflamatoria y neurobiológica, pero no como una intervención contundente ni claramente transformadora por sí sola.
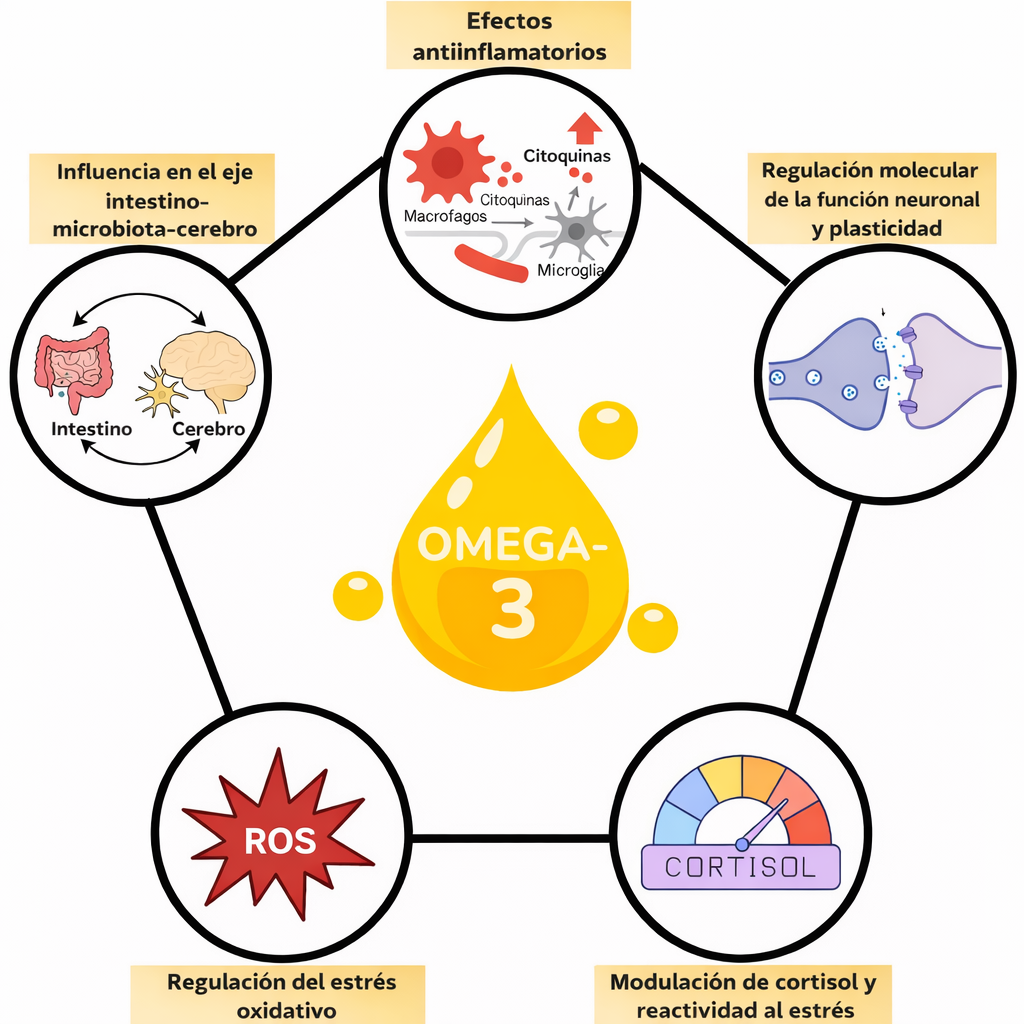
Aunque los omega-3 no parecen ser el “milagro” que a veces se promete para el TDAH, siguen siendo nutrientes relevantes por su participación en procesos como la inflamación, el estrés oxidativo, la respuesta al estrés, la plasticidad neuronal y el eje intestino-microbiota-cerebro. Su valor quizá no esté en un efecto espectacular sobre los síntomas por sí solos, sino en su capacidad para apoyar un terreno biológico más regulado, algo que exploraré con más detalle en próximos artículos.
Figura adaptada de: De Cillis et al., Nutrients, 17(21), 3426, bajo licencia Creative Commons CC BY 4.0.
El azafrán
El azafrán es uno de los suplementos más interesantes en este ámbito, y creo que merece atención seria. Pero también creo que es un buen ejemplo de por qué la metodología importa. El estudio de Baziar de 2019 se cita a menudo porque comparó directamente azafrán con metilfenidato en niños y adolescentes. ⁵ Eso es “clínicamente atrevido” y realmente interesante, pero también hay que verlo por lo que es: un piloto doble ciego de seis semanas en una muestra pequeña y pediátrica. Un resultado positivo en niños no me dice automáticamente que el mismo extracto vaya a comportarse igual en adultos, con un entorno hormonal distinto, otras condiciones coexistentes, otros patrones de sueño, otra exposición a medicación y, sobre todo, otras exigencias vitales. Lo que me dice es que el azafrán merece ser tomado en serio, no que la cuestión en adultos esté ya resuelta.
Un estudio posterior (Blasco-Fontecilla, 2022) es llamativo por otra razón. Utilizó tanto pruebas objetivas como medidas en papel y lápiz, algo que me gusta ver, pero no fue aleatorizado, con metilfenidato en 27 participantes y azafrán en 36, todos entre 7 y 17 años. ⁶ El hallazgo principal fue que el azafrán parecía, en términos generales, comparable al metilfenidato, con el azafrán pareciendo más fuerte para la hiperactividad y el metilfenidato más fuerte para la inatención. Otra señal interesante, pero el diseño no aleatorizado significa que yo tendría cuidado de no tratarlo como algo más robusto de lo que es. Aun así, el equipo de investigación es excelente, y el estudio, desde donde yo lo veo, añade textura a la literatura. Un poco como el azafrán añade color a una buena paella, aunque no sea el ingrediente principal.
El azafrán tiene algo especialmente evocador en el contexto español, y más aún en La Mancha, donde forma parte del paisaje, de la cocina y de la memoria cultural. Aunque probablemente no llegó a la Península exclusivamente a través del mundo árabe, sí parece claro que su expansión y arraigo en España estuvieron muy ligados al periodo andalusí. Me gusta pensar en esto también como un símbolo de algo más amplio: de cómo muchas de las cosas que hoy sentimos profundamente nuestras nacen en realidad del intercambio entre culturas. Quizá por eso el azafrán, además de bello y valioso, tiene algo de puente entre historia, tierra y conocimiento.
El ensayo de azafrán en adultos que me parece más relevante clínicamente, precisamente porque nos obliga a no apoyarnos demasiado en datos infantiles, es el de Pazoki y colegas del 2022. De nuevo, el detalle más importante es que se trata de un ensayo complementario con una muestra de 56 asignados aleatoriamente a recibir Ritalin con azafrán o Ritalin con placebo durante seis semanas, y 44 completaron el estudio. El grupo con azafrán mostró una mayor reducción en la ASRS, con efectos significativos de tiempo por tratamiento también en la Escala de Conners para TDAH en adultos (CAARS). Esto no confirma que el azafrán pueda sustituir al tratamiento estimulante en adultos, pero nos da una indicación de que el metilfenidato combinado con azafrán puede aportar un ángulo de soporte interesante. Es una conclusión estrecha, pero honesta. ⁷
¿Qué es la ASRS?
La ASRS-v1.1 (Adult ADHD Self-Report Scale) es un cuestionario de cribado autoinformado de 18 preguntas, desarrollado por la OMS, diseñado para identificar síntomas de TDAH en adultos (18+ años). Ayuda a detectar signos de inatención e hiperactividad/impulsividad para determinar la necesidad de una evaluación clínica completa. En mi página de orientativa de cribado de TDAH en adultos encontrarás una versión online gratuita que puedes completar para ayudarte a comprender tu neurotipo.
Las revisiones más amplias sobre azafrán son alentadoras, pero también muestran lo temprano que sigue estando este campo. Una revisión sistemática de 2024 sobre azafrán en TDAH incluyó solo cuatro estudios y 118 participantes en total. ⁸ Otra revisión más amplia de 2024 sobre azafrán en condiciones neurológicas y psiquiátricas concluyó que el azafrán no era inferior a fármacos convencionales en varias áreas, incluido el TDAH, pero ese tipo de afirmación puede sonar más decisiva de lo que realmente es el conjunto de datos en TDAH. ⁹ Mi propia lectura es que el azafrán es una de las opciones más creíbles, sobre todo cuando el estado de ánimo, el sueño o la regulación emocional forman parte del cuadro, aunque la evidencia siga siendo todavía limitada.
Veredicto: Azafrán
Para mí, el azafrán es una de las opciones más interesantes y más creíbles de este campo, sobre todo como apoyo bien tolerado, aunque todavía no como un tratamiento plenamente establecido para el TDAH en adultos.
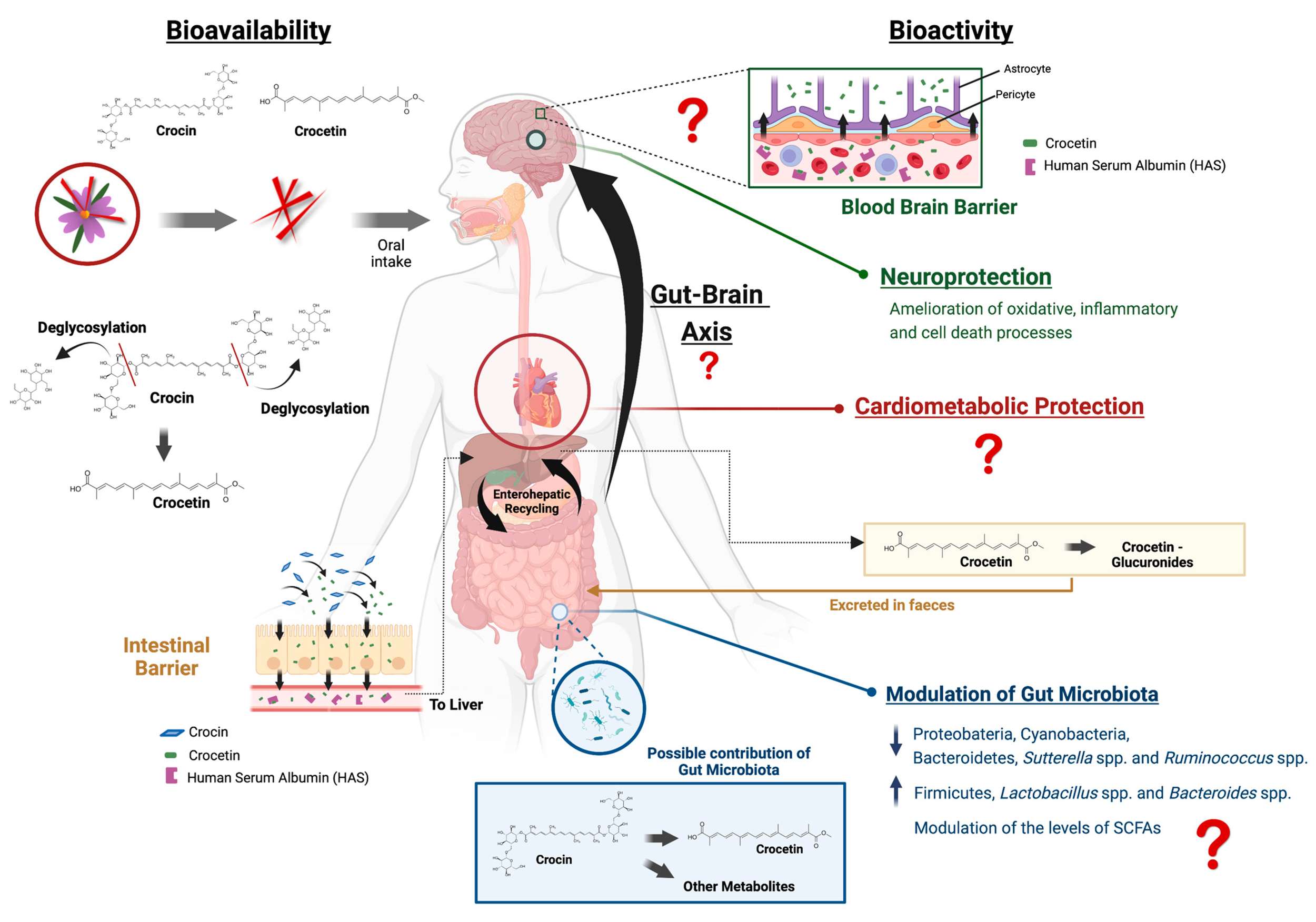
Lo interesante del azafrán no es solo si mejora o no determinados síntomas, sino que parece tocar varios sistemas a la vez: inflamación, neuroprotección, microbiota, barrera intestinal y señalización intestino-cerebro. En un cuadro tan complejo y corporal como el TDAH, ese mapa biológico más amplio también importa. Por estas razones me sigue pareciendo una intervención muy interesante mientras que la evidencia que la sostiene sigue desarrollándose.
Figura reproducida de: Cerdá-Bernad et al., Nutrients, 14(24), 5368, bajo licencia Creative Commons CC BY 4.0.
Como anécdota personal, a raíz de leer estos estudios, yo empecé a tomar azafrán junto con mi metilfenidato diario y he notado que me funciona mejor, con menos picos y valles, de una manera más estable.
El extracto de corteza de pino
El extracto de corteza de pino, normalmente denominado Pycnogenol (aunque esta es una marca registrada), es otro caso interesante, sobre todo porque siempre me pregunto: “¿A quién se le habrá ocurrido pulverizar la corteza de un pino y dársela a alguien como suplemento nutricional para ver qué efectos tenía?”. Me parece a la vez gracioso y alucinante.
La literatura pediátrica sobre el extracto de corteza de pino es más amplia que la literatura en adultos. Uno de los primeros ensayos, publicado en el año 2006, incluyó a 61 niños que recibieron 1 mg/kg/día durante un mes, ¹⁰ y trabajos posteriores, incluido un estudio cruzado doble ciego de 2021 en 20 niños durante dos fases de cuatro semanas con un lavado de dos semanas, siguieron sugiriendo posibles beneficios sobre la inatención, la impulsividad y el equilibrio oxidativo. ¹¹ También hay un ensayo aleatorizado de 2022, de diez semanas, en el que los docentes informaron de mejoras en la puntuación total del TDAH y en la hiperactividad o impulsividad tanto con extracto de corteza de pino como con metilfenidato frente a placebo, mientras que el metilfenidato mostró una ventaja más clara en inatención. ¹² Además, un segundo análisis del mismo ensayo exploró marcadores de estrés oxidativo e inmunidad, así como cambios en apetito y peso. Esto me parece interesante no porque pruebe un mecanismo único y rotundo, sino precisamente porque sirve de recordatorio de que este tipo de compuestos tocan varias capas fisiológicas a la vez. Al mismo tiempo, los propios autores no pudieron confirmar de forma firme una mejora global del estado antioxidante o inmunitario, así que lo leería más como una pista de complejidad biológica que como una demostración mecanística cerrada. ¹³ Mi criterio profesional como investigador es que todo esto merece atención.
El estudio en adultos con corteza de pino, sin embargo, es donde la cuestión de la generalización se vuelve especialmente importante. En el ensayo cruzado de 2002, 24 adultos de entre 24 y 53 años recibieron Pycnogenol, metilfenidato y placebo en orden aleatorizado, cada uno durante tres semanas. ¹⁴ Aunque los síntomas mejoraron durante el tratamiento, ni el metilfenidato ni el Pycnogenol superaron al placebo en las variables principales. Eso no significa que la corteza de pino no sirva para nada. Significa que la evidencia en adultos es escasa y mucho menos clara que la evidencia en niños. También significa que no deberíamos pasar de “prometedor en niños” a “funciona en adultos” como si ese paso no necesitara evidencia propia, aunque esto no niega que el extracto de corteza de pino no tenga una serie de potenciales beneficios que van más allá del cerebro y el sistema nervioso.
Veredicto: Extracto de corteza de pino
Para mí, el extracto de corteza de pino es interesante no solo por lo que podría aportar a algunos síntomas, sino porque apunta a una forma más amplia de apoyo que reconoce que el TDAH no se vive únicamente en el cerebro, sino en todo el cuerpo.
Mi interés por el extracto de corteza de pino en TDAH no se limita a los síntomas nucleares. Como ocurre con otros compuestos bioactivos, su potencial está en la amplitud de sistemas sobre los que parece actuar, desde la función cognitiva y la salud vascular hasta procesos inflamatorios y de regulación más generales. En un cuadro tan corporal como el TDAH, desde donde yo lo veo, eso también merece atención.
Figura adaptada de: Shaw et al., Frontiers in nutrition, 11, 1389374, bajo licencia Creative Commons CC BY 4.0.
La melatonina
La melatonina se entiende mejor, en mi opinión, como un apoyo al sueño y al ritmo circadiano que como un suplemento central para el TDAH, y esta distinción importa. En un estudio abierto en una muestra pequeña de niños y adolescentes con TDAH que ya estaba tomando psicoestimulantes, se comprobó que una pequeña dosis de melatonina (1 mg) puede aumentar el tiempo total de sueño de 463 a 485 minutos en un mes, además de una tendencia a la mejora en otras variables del sueño. ¹⁵ Es un estudio útil, sí, pero no el tipo de diseño a partir del cual yo afirmaría que la melatonina ‘trata el TDAH’. Más bien sugiere un papel de apoyo al sueño en un contexto concreto.
El trabajo de cronoterapia en adultos me parece más interesante porque parte del hecho que en adultos con TDAH hay una mayor susceptibilidad al síndrome de fase de sueño retrasada. En otras palabras, la producción de melatonina empieza más tarde que en personas neurotípicas. Dosis bajas de melatonina parecen adelantar el ritmo circadiano, reduciendo hasta un 14% los síntomas autoinformados de TDAH inmediatamente después de la suplementación, aunque el efecto se desvanece pocas semanas después de terminar el tratamiento. ¹⁶ Esto me dice dos cosas. Primero, que parte del sufrimiento asociado al TDAH es, en algunos casos, un problema de ritmo. Segundo, que la melatonina es más relevante cuando el retraso de fase circadiana forma realmente parte del cuadro, no como intervención universal para todas las personas con TDAH.
La revisión más amplia sobre intervenciones del sueño en niños apunta en la misma dirección, es decir, que las intervenciones sobre el sueño pueden mejorar el sueño y, a veces, variables relacionadas con el TDAH, pero que la evidencia es heterogénea. ¹⁷ Esta revisión me parece valiosa porque nos saca del reflejo de pensar el sueño como una cuestión secundaria en el TDAH. Lo que deja ver es que, cuando el sueño mejora, no solo puede mejorar el descanso, sino también la calidad de vida y, en algunos casos, ciertos aspectos del propio cuadro clínico. También me gusta porque, al ser una revisión, no vende soluciones limpias ni universales: más bien muestra un campo útil, prometedor y todavía bastante heterogéneo.
Veredicto: Melatonina
Para mí, la melatonina tiene más sentido cuando el sueño y el ritmo circadiano forman parte del problema, más como apoyo regulador de la relación cuerpo-mente que como tratamiento directo del TDAH. Yo la tomo y siento que me ayuda a descansar mejor. Esto es lo que yo creo que me beneficia, más que un efecto específico sobre mis síntomas.
La L-teanina
Si seguimos hablando de ritmos circadianos, sueño y descanso, yo recomiendo que se aplique la misma cautela a la L-teanina. Entiendo por qué atrae a tantas personas. Se sitúa en ese espacio de calma sin sedación que muchos de los que vivimos con TDAH vamos buscando, aunque la evidencia en este campo sigue siendo estrecha. En uno de los ensayos más conocidos, la suplementación con 400 mg diarios ayudó a mejorar algunos aspectos de la calidad objetiva del sueño en niños con TDAH. Niños, no adultos, y calidad del sueño más que el cuadro general del TDAH. ¹⁸
Además, una revisión sistemática publicada en el 2024 sobre L-teanina en trastornos mentales confirma que este aminoácido presente en el té verde puede ayudar como complemento en situaciones en las que el sueño deficiente, la sobreestimulación o la reactividad al estrés forman parte del cuadro, pero no como un tratamiento principal basado en evidencia para el TDAH en adultos. ¹⁹
Veredicto: L-teanina
Para mí, la L-teanina es más un apoyo suave para favorecer un terreno interno algo más calmado, más regulado y quizá un poco más habitable, que una intervención principal para el TDAH en adultos.
Personalmente, yo soy “team L-teanina” y la tomo todas las tardes/noches desde hace años.
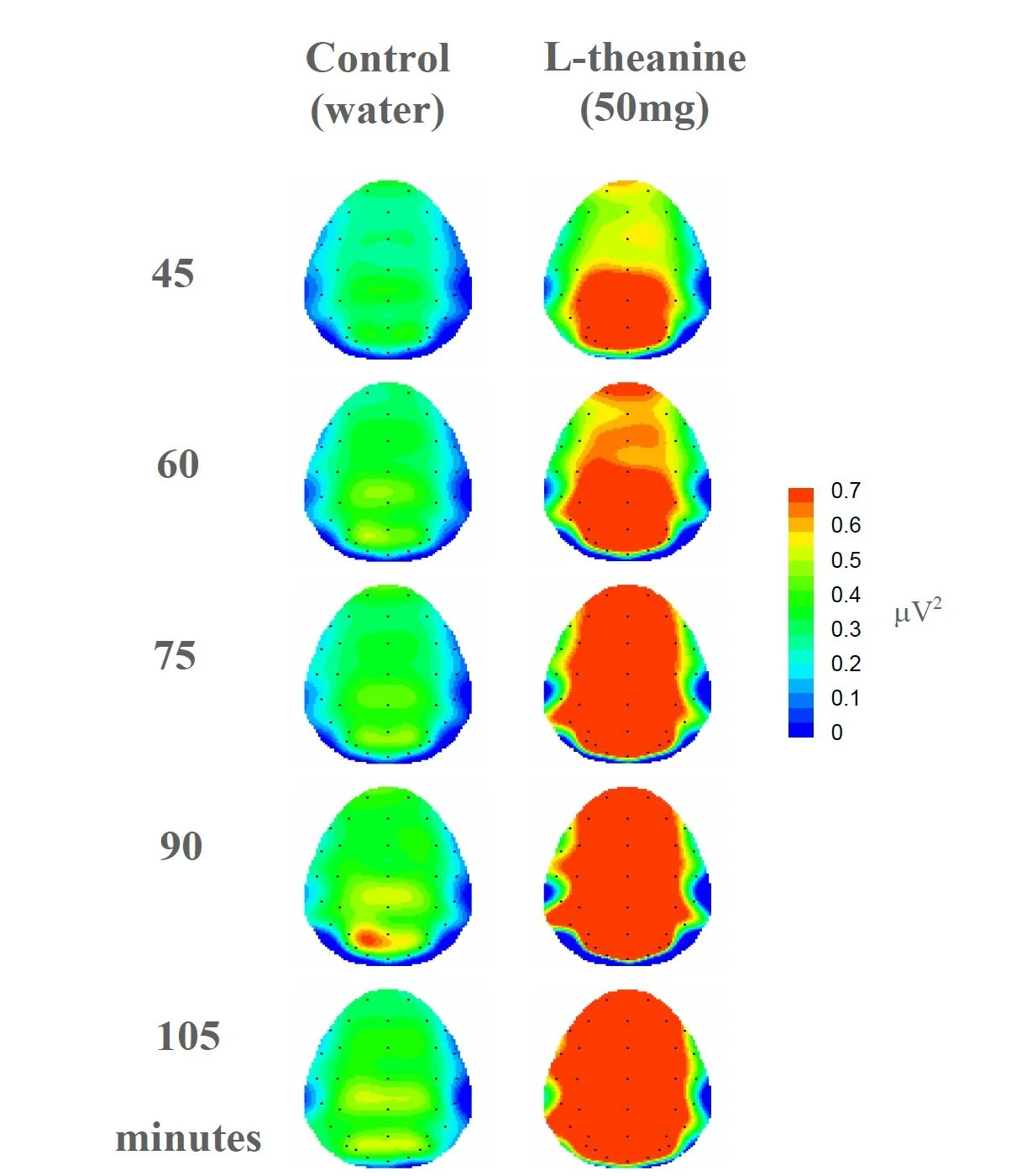
Más que “tranquilizar” sin más, la L-teanina parece favorecer un estado de calma con cierto grado de alerta, como refleja el aumento de actividad alfa-1 observado aquí. En un cuadro como el TDAH, donde el problema no siempre es falta de activación sino a veces una activación mal acompasada, este matiz importa.
Rojo = más actividad alfa-1; verde = menos actividad alfa-1. En este estudio, más rojo tras tomar L-teanina sugiere un estado de calma alerta, no de somnolencia.
Figura adaptada de: Nobre et al., Asia Pac J Clin Nutr.2008:17 Suppl 1:167-8, bajo licencia Creative Commons CC BY 4.0.
La vitamina D
La vitamina D es uno de esos nutrientes en los que la señal observacional parece más consistente que la señal de intervención. Varios metaanálisis muestran que niños y adolescentes con TDAH tienden a presentar concentraciones séricas de 25(OH)D (vitamina D3) más bajas que los controles, lo que la convierte en un nutriente al que merece la pena prestar atención. Pero eso no significa, por sí solo, que la vitamina D baja esté causando el TDAH de una manera simple y directa. La mayor parte de esta literatura es pediátrica, y unos niveles bajos también pueden reflejar menos tiempo al aire libre, el momento del año, adiposidad, calidad de la dieta, sueño o patrones generales de salud que acompañan al TDAH, en lugar de situarse claramente como desencadenante causal. Por eso, a mí me parece una asociación interesante, pero no autoexplicativa.
Donde la historia de la vitamina D se vuelve más relevante clínicamente es en los ensayos de suplementación, aunque también aquí creo que a veces se sobredimensionan los hallazgos. El metaanálisis de Gan y colaboradores, publicado en 2019, agrupó cuatro ensayos clínicos aleatorizados, con 256 niños en total, y encontró mejoras pequeñas pero estadísticamente significativas en síntomas totales de TDAH, inatención, hiperactividad y conducta. ²⁰ Para mí, el detalle metodológico clave, sin embargo, es que estos estudios incluidos en esta revisión son ensayos coadyuvantes, es decir, estudios donde la vitamina D se añadió al metilfenidato, no intervenciones donde la vitamina D fue utilizada como tratamiento único. Además, los propios autores fueron prudentes: la evidencia seguía siendo limitada y no se observaron mejoras claras en los problemas de conducta más desafiantes o confrontativos. Yo lo leería, por tanto, como una señal modesta de posible utilidad como complemento en población infantil, no como una prueba de que la vitamina D “trate el TDAH” de forma independiente.
El ensayo de Elshorbagy y colaboradores también es llamativo porque informó de mejoras en función cognitiva y en varios dominios sintomáticos en niños con TDAH tras suplementación con vitamina D. ²¹ Pero, de nuevo, se trata de un estudio pediátrico, y como ocurre con el resto de esta literatura, no resuelve la cuestión en adultos. Esa es la parte que yo seguiría subrayando. Todavía no tenemos datos robustos de suplementación en adultos, así que no me parece científicamente cuidadoso extrapolar de forma directa desde ensayos en niños a adultos con una fisiología distinta, más condiciones coexistentes como ansiedad, depresión, y trastornos conductuales de la alimentación, otro uso de medicación y otras presiones vitales.
Mi sensación actual es que la vitamina D tiene más sentido como intervención guiada por el estado nutricional y la posibilidad de déficit, especialmente cuando unos niveles bajos son plausibles, que como suplemento general para cualquier persona con TDAH. La revisión paraguas de 2024 de Kitaneh y colaboradores también va en esa dirección: hay una relación plausible entre vitamina D y TDAH, pero sigue habiendo heterogeneidad y necesidad de estudios mejores, especialmente fuera de la población infantil. ²²
Veredicto: Vitamina D
Para mí, la vitamina D tiene más sentido como marcador de terreno fisiológico que conviene revisar cuando hay razones para sospechar niveles bajos, que como suplemento general para cualquier persona con TDAH.
El magnesio
El magnesio es un caso algo distinto. Aquí, la literatura sobre “estado” nutricional es, probablemente, más consistente que la literatura de intervención. Dos metaanálisis encontraron que los niños con TDAH tienden a mostrar niveles séricos de magnesio más bajos, ²³ y uno de ellos también observó niveles más bajos en cabello. ²⁴ Aunque eso aporte una señal bioquímica plausible, la literatura sobre magnesio es más desordenada metodológicamente de lo que parece. Los estudios no miden todos lo mismo: suero, plasma, cabello, saliva, eritrocitos u orina, y esas matrices no cuentan exactamente la misma historia. Una revisión crítica de Robberecht y colaboradores explican bien este punto al señalar que el magnesio intracelular podría ser un indicador más útil que el sérico aislado, y que la propia medicación estimulante podría influir en los niveles circulantes. ²⁵ Es decir, incluso antes de hablar de suplementación, la cuestión del biomarcador ya es menos limpia de lo que sugieren algunos titulares.
Lo que me mantiene más prudente es que la literatura de suplementación es más difícil de interpretar que la literatura sobre niveles. Por ejemplo, la revisión de Robberecht también señala como muchos ensayos con magnesio no son ensayos “puros”, porque se el mineral se administró junto con omega-3, zinc u otros nutrientes. Eso hace muy difícil atribuir un efecto a un solo componente. Otros estudios han llegado a conclusiones parecidas ya hace algunos años: el magnesio puede ayudar a algunos niños con TDAH, sobre todo cuando hay deficiencia o alto riesgo de deficiencia, pero la evidencia no es lo bastante sólida como para justificar una recomendación rutinaria. ²⁶ En otras palabras, el magnesio me parece plausible, potencialmente relevante y digno de ser evaluado, pero todavía no lo presentaría como un tratamiento ampliamente respaldado por evidencia para el TDAH en sí mismo.
Otra cosa a destacar aquí es la laguna en adultos. La mayor parte de la literatura sobre magnesio sigue siendo pediátrica, y los datos más recientes en muestras comunitarias siguen siendo preliminares. El artículo de Hunter y colaboradores de 2025 es útil porque intenta ampliar la mirada más allá de la infancia, pero era una muestra pequeña y mixta de personas neurodivergentes, con solo 10 adultos, y no un ensayo de intervención específico en TDAH. ²⁷ Esto lo hace valioso para generar una hipótesis, pero no para respaldar afirmaciones firmes de tratamiento.
Veredicto: Magnesio
Para mí, el magnesio merece atención sobre todo en contexto, especialmente cuando hay alimentación restrictiva, selectividad sensorial, mal sueño, estrés crónico o menor ingesta, más que como tratamiento específico del TDAH en sí mismo.
¿Quieres saber más sobre qué alimentos son ricos en magnesio? Lee este artículo de la Universidad de Navarra: Alimentos ricos en magnesio.
La microbiota, los probióticos y los alimentos fermentados
La literatura sobre intestino y cerebro es fascinante, pero este es uno de los ámbitos más fáciles de exagerar. Y créeme porque este es el campo en el que llevo trabajando muchos años y cada vez oigo y leo más barbaridades con muy poco fundamento científico.
La revisión sistemática de 2024 de Allahyari y colaboradores concluyó que los probióticos y prebióticos pueden ser beneficiosos como terapias adyuvantes en TDAH, pero también pide estudios más largos, con más participantes, una gama más amplia de edades y métodos de evaluación más variados. ²⁸ Ese me parece un resumen justo del punto en el que estamos. Hay promesa, pero también muchas cosas que todavía no sabemos.
Los datos en adultos siguen siendo especialmente escasos. Un buen ejemplo es una revisión sistemática del 2025 sobre modulación de la microbiota intestinal en adultos con TDAH que acabó incluyendo solo tres ensayos clínicos aleatorizados. ²⁹ Entre esos trabajos, el ensayo doble ciego en adultos de Schwartz y colaboradores, publicado en 2024, resulta especialmente interesante porque informó de menos hiperactividad, menos síntomas gastrointestinales y mejor rendimiento académico tras la intervención probiótica, siendo la menor edad uno de los predictores de una respuesta más favorable. ³⁰
Dicho esto, cuando hablamos de microbiota no todo tiene por qué reducirse a un probiótico en cápsulas. En mi propio trabajo de investigación, he explorado también intervenciones dirigidas a la microbiota a través de la alimentación y de alimentos fermentados como el kéfir. Me interesa especialmente ese enfoque porque se aleja de la idea de una cepa milagrosa y se acerca más a una ecología intestinal vivida, comestible y potencialmente más integrada con la vida real.
Primero publicamos un estudio de viabilidad en la revista Pilot and Feasibility Studies, en el que probamos una intervención dietética dirigida a la microbiota en niños con TDAH y observamos que el enfoque era seguro, tolerable y factible, con buena adherencia y señales suficientes como para justificar un ensayo mayor. ³¹ Después publicamos en BMJ Open el protocolo del ensayo aleatorizado sobre kéfir, conducta, sueño y microbioma, precisamente para estudiar de forma más rigurosa ese tipo de intervención alimentaria.³² Más recientemente, los resultados del ensayo clínico se publicaron en BMC Psychiatry. ³³ No creo que estos trabajos cierren el caso, ni mucho menos, pero sí ayudan a ampliar la conversación. Quizá el futuro de este campo no esté solo en suplementos aislados, sino también en formas más amplias y más alimentarias de modular el eje intestino-cerebro.
Veredicto: Probióticos
Para mí, este es un campo muy prometedor y biológicamente fascinante, pero todavía demasiado heterogéneo y preliminar como para hablar de soluciones universales; lo más interesante quizá no sea una cepa concreta, sino una forma más ecológica y alimentaria de modular el eje intestino-cerebro.
A fin de cuentas… Una herramienta más, no una solución
Todo esto es una de las razones por las que vuelvo una y otra vez a la imagen más amplia. Una cápsula puede apoyar una capa del sistema pero, por muy tentador que sea o por mucho que te lo vendan como parte de un protocolo “premium”, nunca podrá ser el sistema entero. Te pongo un ejemplo muy breve para ilustrar lo que quiero decir. El movimiento importa, no simplemente porque el ejercicio sea “saludable”, sino porque cambia la fisiología de maneras relevantes para la regulación. Revisiones recientes sugieren que el ejercicio puede aumentar la diversidad microbiana en adultos, potenciar la producción de ácidos grasos de cadena corta y apoyar la adaptación y la biogénesis mitocondrial. ³⁴ ³⁵ En otras palabras, el movimiento no va solo de músculos. Va de energía, de señalización intestino-cerebro y de cambio de estado. Esa es una conversación muy distinta, a la vez que mucho más verdadera, de la de “sal a correr y se te arreglará el TDAH”.
Entonces, con tanta cautela, ¿dónde nos deja todo esto? Desde donde escribo, podré parecer cauteloso, sí, pero te aseguro también que me siento esperanzado. Creo que merece la pena seguir de cerca el azafrán, que la corteza de pino es muy interesante, especialmente en TDAHeros más jóvenes, y que la melatonina puede ser muy relevante cuando los desarreglos del sistema nervioso afectan al horario del sueño. También creo que la vitamina D y el magnesio tienen más sentido cuando es plausible que haya niveles bajos, y que la L-teanina puede ayudar a algunas personas, sobre todo en relación con la sobreestimulación. Y, por supuesto, habiéndome especializado en la microbiota y la salud mental, me parece que este campo es apasionante, pero tengo que reconocer que es todavía joven. Sobre todo, creo que los suplementos pueden apoyar un plan más amplio, pero que no pueden ser el plan. Y eso te lo digo tanto como investigador, como clínico y como persona neurodivergente que lleva muchísimos años probándolo todo.
Así que, para terminar, no me parece que la pregunta sea “¿qué suplemento arregla el TDAH?”, sino “¿qué necesita apoyo en mi cuerpo y mi mente, y qué puede aportar realmente esta herramienta?”. Es una pregunta menos vistosa, pero mucho más útil porque deja el espacio necesario para que la medicación, la terapia, la alimentación, el movimiento, la creatividad y la autocompasión formen parte de la misma conversación, que es donde yo creo que deben estar.
Con cariño,
Si estás intentando decidir con más criterio qué papel pueden tener los suplementos, la alimentación, la medicación u otras formas de apoyo en tu caso concreto, en mi página de acompañamiento encontrarás información sobre cómo trabajo en consulta.
Nota importante: Esta revisión nace de mi interés profesional y de investigación en el campo, así como de mi experiencia educativa y clínica. Si estás considerando alguno de estos suplementos en el contexto de una condición médica o de un tratamiento farmacológico, consúltalo antes con tu médico o con un dietista-nutricionista cualificado.
Referencias: La ciencia que informa este artículo
National Institute for Health and Care Excellence. (2018, actualizado 2019). Attention deficit hyperactivity disorder: Diagnosis and management (NICE Guideline NG87).https://www.nice.org.uk/guidance/ng87
Notas: Esta guía clínica del NICE (Reino Unido) establece recomendaciones basadas en evidencia para el diagnóstico y tratamiento del TDAH a lo largo de la vida. Destaca que el tratamiento farmacológico, incluyendo metilfenidato y lisdexanfetamina en adultos, debe integrarse dentro de un plan terapéutico más amplio y personalizado.
Gillies, D., Leach, M. J., & Perez Algorta, G. (2023). Polyunsaturated fatty acids (PUFA) for attention deficit hyperactivity disorder (ADHD) in children and adolescents. The Cochrane database of systematic reviews, 4(4), CD007986. https://doi.org/10.1002/14651858.CD007986.pub3
Notas: Este estudio es importante porque actúa como un necesario contrapeso frente al entusiasmo que suele rodear a los omega-3 en el TDAH. Al tratarse de una revisión Cochrane, aporta una lectura especialmente rigurosa y prudente de la evidencia disponible en niños y adolescentes, y nos recuerda que “muy investigado” no es lo mismo que “claramente eficaz”. En el contexto de este artículo, ayuda a situar los omega-3 en un lugar más honesto: como un apoyo potencial dentro de un abordaje más amplio, no como una solución contundente ni fácilmente extrapolable a adultos.
Liu, T.-H., Wu, J.-Y., Huang, P.-Y., Lai, C.-C., Chang, J. P.-C., Lin, C.-H., & Su, K.-P. (2023). Omega-3 polyunsaturated fatty acids for core symptoms of attention-deficit/hyperactivity disorder: A meta-analysis of randomized controlled trials. Journal of Clinical Psychiatry, 84(5), 22r14772. https://doi.org/10.4088/JCP.22r14772
Notas: Lo interesante de este metaanálisis es que la posible ventaja de los omega-3 apareció solo en los ensayos más largos, de al menos 4 meses, refiriéndose a los síntomas nucleares del TDAH en conjunto como una señal modesta dentro del propio cuadro clínico del TDAH. Al mismo tiempo, el estudio no permite afirmar con claridad qué dimensión concreta, inatención, hiperactividad o impulsividad, fue la que más se benefició de esa mayor duración.
Chang, J. P., Su, K. P., Mondelli, V., & Pariante, C. M. (2018). Omega-3 Polyunsaturated Fatty Acids in Youths with Attention Deficit Hyperactivity Disorder: a Systematic Review and Meta-Analysis of Clinical Trials and Biological Studies. Neuropsychopharmacology : official publication of the American College of Neuropsychopharmacology, 43(3), 534–545. https://doi.org/10.1038/npp.2017.160
Notas: El estudio de Chang et al. es importante porque introduce un matiz necesario en una literatura que, vista solo desde las revisiones más recientes, podría parecer más negativa de lo que realmente es. Su valor está en que detecta una señal favorable en niños y adolescentes, tanto en síntomas clínicos como en algunas medidas de atención, y además aporta plausibilidad biológica al mostrar niveles más bajos de DHA y EPA en jóvenes con TDAH. Este estudio ayuda a sostener una postura equilibrada: los omega-3 no parecen una intervención contundente, pero tampoco pueden descartarse como irrelevantes, sobre todo en población más joven y quizá en ensayos de mayor duración.
Baziar, S., Aqamolaei, A., Khadem, E., Mortazavi, S. H., Naderi, S., Sahebolzamani, E., Mortezaei, A., Jalilevand, S., Mohammadi, M. R., Shahmirzadi, M., & Akhondzadeh, S. (2019). Crocus sativus L. Versus Methylphenidate in Treatment of Children with Attention-Deficit/Hyperactivity Disorder: A Randomized, Double-Blind Pilot Study. Journal of child and adolescent psychopharmacology, 29(3), 205–212. https://doi.org/10.1089/cap.2018.0146
Notas: Este estudio es importante porque fue uno de los primeros ensayos en comparar directamente azafrán y metilfenidato en población infantil con TDAH, utilizando un diseño aleatorizado y doble ciego. Su principal interés está en que sugiere una posible eficacia comparable a corto plazo, pero al tratarse de un estudio piloto, con una muestra pequeña y solo en niños y adolescentes, sus resultados deben leerse como una señal prometedora, no como una prueba definitiva ni fácilmente extrapolable a adultos. Por eso insisto en que la metodología y la demografía de la muestra siempre son claves para no exagerar los resultados de un estudio, por muy buena pinta que tenga.
Blasco-Fontecilla, H., Moyano-Ramírez, E., Méndez-González, O., Rodrigo-Yanguas, M., Martin-Moratinos, M., & Bella-Fernández, M. (2022). Effectivity of Saffron Extract (Saffr'Activ) on Treatment for Children and Adolescents with Attention Deficit/Hyperactivity Disorder (ADHD): A Clinical Effectivity Study. Nutrients, 14(19), 4046. https://doi.org/10.3390/nu14194046
Notas: Un estudio sugerente porque explora el potencial del azafrán en niños y adolescentes con TDAH e incorpora medidas más objetivas que muchos trabajos similares. Aun así, su diseño no aleatorizado obliga a interpretarlo con prudencia: aporta una señal interesante, pero no una prueba definitiva ni fácilmente extrapolable a adultos.
Pazoki, B., Zandi, N., Assaf, Z., Sanjari Moghaddam, H., Zeinoddini, A., Mohammadi, M. R., & Akhondzadeh, S. (2022). Efficacy and safety of saffron as adjunctive therapy in adults with attention-deficit/hyperactivity disorder: A randomized, double-blind, placebo-controlled clinical trial. Advances in Integrative Medicine, 9(1), 37–43. https://doi.org/10.1016/j.aimed.2022.01.002
Notas: Este estudio me parece especialmente relevante porque desplaza la conversación sobre el azafrán desde la infancia hacia la población adulta, algo que sigue siendo poco frecuente en este campo. Además, no evalúa el azafrán como sustituto de la medicación, sino como complemento a metilfenidato, lo cual hace que la pregunta clínica sea más realista. Su principal valor está en que ofrece una señal prometedora en adultos dentro de un diseño aleatorizado, doble ciego y controlado con placebo. Al mismo tiempo, sigue siendo un estudio pequeño y de corta duración, así que yo lo leería como una prueba de concepto interesante, no como una confirmación definitiva de eficacia.
Seyedi-Sahebari, S., Farhang, S., Araj-Khodaei, M., Akhondzadeh, S., Naseri, A., Sanaie, S., & Frounchi, N. (2024). The Effects of Crocus sativus (Saffron) on ADHD: A Systematic Review. Journal of attention disorders, 28(1), 14–24. https://doi.org/10.1177/10870547231203176
Notas: Una revisión pequeña, sí, pero útil precisamente por eso. Porque nos recuerda que el entusiasmo con el azafrán en TDAH todavía se apoya en un puñado de estudios, no en una montaña de evidencia. Prometedor, sí; maduro, todavía no. Pero con una tolerabilidad que, hasta ahora, parece razonablemente buena. Y como es una intervención basada en un alimento usado tradicionalmente, si las expectativas son adecuadas, es una manera poco arriesgada de experimentar.
Han, S., Cao, Y., Wu, X., Xu, J., Nie, Z., & Qiu, Y. (2024). New horizons for the study of saffron (Crocus sativus L.) and its active ingredients in the management of neurological and psychiatric disorders: A systematic review of clinical evidence and mechanisms. Phytotherapy research : PTR, 38(5), 2276–2302. https://doi.org/10.1002/ptr.8110
Notas: Esta revisión es interesante porque amplía mucho el foco y sitúa el TDAH dentro de un mapa clínico más amplio. Justamente por eso conviene leerla con cuidado: cuando el zoom se aleja mucho, el detalle específico del TDAH puede parecer más sólido de lo que realmente es.
Trebatická, J., Kopasová, S., Hradecná, Z., Cinovský, K., Skodácek, I., Suba, J., Muchová, J., Zitnanová, I., Waczulíková, I., Rohdewald, P., & Duracková, Z. (2006). Treatment of ADHD with French maritime pine bark extract, Pycnogenol. European child & adolescent psychiatry, 15(6), 329–335. https://doi.org/10.1007/s00787-006-0538-3.
Notas: Este ensayo tiene valor casi histórico dentro de este pequeño nicho, porque ayudó a poner el extracto de corteza de pino en el mapa del TDAH bastante antes de que este tema estuviera “de moda”. También resulta interesante que ya entonces apuntara hacia el estrés oxidativo como parte del cuadro, algo que hoy encaja bastante bien con lecturas más sistémicas y menos reduccionistas del TDAH algo que hoy encaja bastante bien con lecturas más sistémicas del TDAH, en las que la inflamación y el estrés oxidativo se consideran capas potencialmente relevantes.
Hsu, C. D., Hsieh, L. H., Chen, Y. L., Lin, I. C., Chen, Y. R., Chen, C. C., Shirakawa, H., & Yang, S. C. (2021). Complementary effects of pine bark extract supplementation on inattention, impulsivity, and antioxidative status in children with attention-deficit hyperactivity disorder: A double-blinded randomized placebo-controlled cross-over study. Phytotherapy research : PTR, 35(6), 3226–3235. https://doi.org/10.1002/ptr.7036
Notas: Lo más atractivo de este estudio no es solo el diseño cruzado, que permite que cada niño actúe en parte como su propio control, sino el intento de conectar conducta y estado antioxidante en el mismo trabajo. Me parece un buen ejemplo de esa intuición que atraviesa todo este artículo: a veces los cambios más interesantes no ocurren en un solo nivel, sino en la conversación entre síntomas, biología y contexto.
Weyns, A.-S., Verlaet, A. A. J., Breynaert, A., Naessens, T., Fransen, E., Verhelst, H., Van West, D., Van Ingelghem, I., Jonckheere, A. I., Beysen, D., Kenis, S., Moens, E., van Roest, A. P. J., Savelkoul, H. F. J., De Bruyne, T., Pieters, L., Ceulemans, B., & Hermans, N. (2022). Clinical investigation of French maritime pine bark extract on attention-deficit hyperactivity disorder as compared to methylphenidate and placebo: Part 1: Efficacy in a randomised trial. Journal of Functional Foods, 97, 105246. https://doi.org/10.1016/j.jff.2022.105246
Notas: Este estudio me parece especialmente útil porque introduce una comparación más exigente de lo habitual: no solo frente a placebo, sino también frente a metilfenidato. Y eso obliga a situar el extracto de corteza de pino en un terreno más clínico y menos idealizado. No lo convierte en “sustituto” de nada, pero sí lo saca del cajón de lo meramente especulativo.Weyns, A.-S., Verlaet, A. A. J., Van Herreweghe, M., Breynaert, A., Fransen, E., De Meester, I., Logie, E., Vanden Berghe, W., Verhelst, H., Van West, D., Van Ingelghem, I., Jonckheere, A. I., Beysen, D., Kenis, S., Moens, E., van Roest, A. P. J., Savelkoul, H. F. J., De Bruyne, T., Pieters, L., Ceulemans, B., & Hermans, N. (2022). Clinical investigation of French maritime pine bark extract on attention-deficit hyperactivity disorder as compared to methylphenidate and placebo: Part 2: Oxidative stress and immunological modulation. Journal of Functional Foods, 97, 105247. https://doi.org/10.1016/j.jff.2022.105247
Notas: Este segundo artículo de Weyns y colegas me gusta porque complica la historia, y como buen TDAHero, ¡me alucina una historia complicada! :) Sobre todo porque, en este caso, complicarla es una virtud. En lugar de confirmar un mecanismo bonito y limpio, muestra lo difícil que es demostrar de forma robusta que un compuesto actúa exactamente donde intuimos que podría actuar. La biología suele ser más enmarañada y menos elegante que las hipótesis que los científicos nos planteamos y, precisamente por eso, resulta más creíble.Tenenbaum, S., Paull, J. C., Sparrow, E. P., Dodd, D. K., & Green, L. (2002). An experimental comparison of Pycnogenol and methylphenidate in adults with Attention-Deficit/Hyperactivity Disorder (ADHD). Journal of attention disorders, 6(2), 49–60. https://doi.org/10.1177/108705470200600201.
Notas: Este estudio es importante porque es uno de los pocos ensayos que analiza el extracto de corteza de pino en adultos con TDAH. Sus resultados no fueron especialmente convincentes, ya que ni el Pycnogenol ni el metilfenidato superaron claramente al placebo en las variables principales. Para mí, eso no significa que debamos descartar por completo el extracto de corteza de pino, pero sí nos recuerda que la evidencia en adultos sigue siendo escasa, y que los hallazgos prometedores en niños no pueden trasladarse sin más al TDAH en adultos sin estudios adecuados.
Checa-Ros, A., Muñoz-Hoyos, A., Molina-Carballo, A., Viejo-Boyano, I., Chacín, M., Bermúdez, V., & D'Marco, L. (2023). Low Doses of Melatonin to Improve Sleep in Children with ADHD: An Open-Label Trial. Children (Basel, Switzerland), 10(7), 1121. https://doi.org/10.3390/children10071121
Notas: Este estudio me parece útil porque pone el foco en algo que a menudo queda en segundo plano en el TDAH, el sueño. También recuerda que mejorar el descanso puede ser clínicamente relevante aunque no estemos “tratando el TDAH” de forma directa. Al ser un estudio abierto, yo lo leería como una señal inicial interesante, más orientada a abrir preguntas buenas que a cerrar conclusiones.van Andel, E., Bijlenga, D., Vogel, S. W. N., Beekman, A. T. F., & Kooij, J. J. S. (2021). Effects of chronotherapy on circadian rhythm and ADHD symptoms in adults with attention-deficit/hyperactivity disorder and delayed sleep phase syndrome: a randomized clinical trial. Chronobiology international, 38(2), 260–269. https://doi.org/10.1080/07420528.2020.1835943
Notas: Este estudio me parece especialmente valioso porque desplaza la conversación desde el “déficit de atención” hacia algo mucho más basal y corporal, el ritmo circadiano. En adultos con TDAH y síndrome de fase de sueño retrasada, recuerda que a veces parte del sufrimiento no está solo en la atención en sí, sino en vivir fisiológicamente desacompasados. También me gusta porque no presenta la cronoterapia como una solución mágica, sino como una vía interesante para pensar el TDAH desde la temporalidad, el sueño y la regulación, algo de lo que hablo en mi libro Cuerpo y Mente TDAH.Larsson, I., Aili, K., Lönn, M., Svedberg, P., Nygren, J. M., Ivarsson, A., & Johansson, P. (2023). Sleep interventions for children with attention deficit hyperactivity disorder (ADHD): A systematic literature review. Sleep medicine, 102, 64–75. https://doi.org/10.1016/j.sleep.2022.12.021
Notas: Una revisión especialmente útil porque recuerda que intervenir sobre el sueño no es “tratar algo aparte”, sino trabajar sobre una capa muy relevante para los que vivimos con TDAH. Su principal fuerza está en poner orden en un campo prometedor, pero todavía desigual y un tanto enmarañado en cuanto a métodos y resultados.Lyon, M. R., Kapoor, M. P., & Juneja, L. R. (2011). The effects of L-theanine (Suntheanine®) on objective sleep quality in boys with attention deficit hyperactivity disorder (ADHD): a randomized, double-blind, placebo-controlled clinical trial. Alternative medicine review : a journal of clinical therapeutic, 16(4), 348–354.
Notas: Este estudio me parece interesante porque sitúa la L-teanina en un lugar más realista y, para mí, más útil: no tanto como “suplemento para el TDAH” en sentido amplio, sino como posible apoyo para una capa concreta del cuadro, el sueño. También recuerda algo importante en este artículo: a veces mejorar el descanso no resuelve el TDAH, pero sí puede suavizar bastante la experiencia de vivir con él. Yo llevo tiempo tomando 400mg cada tarde/noche.Moshfeghinia, R., Sanaei, E., Mostafavi, S., Assadian, K., Sanaei, A., & Ayano, G. (2024). The effects of L-theanine supplementation on the outcomes of patients with mental disorders: a systematic review. BMC psychiatry, 24(1), 886. https://doi.org/10.1186/s12888-024-06285-y
Notas: Esta revisión me parece útil porque coloca la L-teanina en un lugar más realista: no como solución estrella, sino como apoyo suave y potencialmente interesante en cuadros donde la ansiedad, la sobreestimulación o el mal sueño forman parte del problema. También viene bien para recordar que tenemos que ser bastante prudentes al extrapolar desde “trastornos mentales” en general al TDAH en adultos.Gan, J., Galer, P., Ma, D., Chen, C. y Xiong, T. (2019). The Effect of Vitamin D Supplementation on Attention-Deficit/Hyperactivity Disorder: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Journal of Child and Adolescent Psychopharmacology, 29(9), 670–687.
Notas: Un metaanálisis importante porque ayuda a aterrizar la conversación sobre vitamina D: hay una señal pequeña a favor, sí, pero en ensayos pediátricos y como complemento al metilfenidato, no como tratamiento independiente. Su principal valor está en obligarnos a distinguir entre una ayuda coadyuvante plausible y una intervención principal, que sería decir demasiado. Elshorbagy, H.H., Barseem, N.F., Abdelghani, W.E. et al. (2018). Impact of Vitamin D Supplementation on Attention-Deficit Hyperactivity Disorder in Children. Annals of Pharmacotherapy, 52(7), 623–631.
Notas: Este estudio resulta interesante porque apunta a mejoras cognitivas y conductuales tras suplementación con vitamina D en niños, pero también porque ilustra bien uno de los límites recurrentes de este campo: los resultados son sugerentes en población pediátrica, sin resolver por ello la gran pregunta de si algo parecido ocurre en adultos. Es un estudio que abre una puerta, no que cierre el debate.Kitaneh, R., Jalilian-Khave, L., Ysrayl, B.B. et al. (2024). The Relationship Between Vitamin D and the Development and Treatment of Attention-Deficit Hyperactivity Disorder: An Overview of Systematic Reviews. Current Behavioral Neuroscience Reports, 11(3), 164–181.
Notas: Esta revisión paraguas me parece especialmente útil porque no intenta simplificar una literatura que sigue siendo bastante heterogénea. Más que vender una conclusión rotunda, ayuda a situar la vitamina D donde probablemente corresponde ahora mismo: como un factor biológicamente plausible y clínicamente interesante, pero todavía lejos de justificar un entusiasmo excesivo.Effatpanah, M., Rezaei, M., Effatpanah, H. et al. (2019). Magnesium status and attention deficit hyperactivity disorder (ADHD): A meta-analysis. Psychiatry Research, 274, 228–234.
Notas: Un metaanálisis útil porque refuerza la idea de que el magnesio merece atención como marcador biológico, aunque no necesariamente como solución terapéutica en sí misma. También es una buena advertencia contra las lecturas rápidas: la señal existe, pero la heterogeneidad entre estudios sigue siendo demasiado alta como para sacar conclusiones facilonas.Huang, Y.H., Zeng, B.Y., Li, D.J. et al. (2019). Significantly lower serum and hair magnesium levels in children with attention deficit hyperactivity disorder than controls: A systematic review and meta-analysis. Progress in Neuro-Psychopharmacology and Biological Psychiatry, 90, 134–141.
Notas: Lo más valioso de esta revisión, para mí, es que amplía la conversación más allá del suero e incluye también niveles en cabello, recordándonos que el “estado de magnesio” no siempre se deja capturar por un solo biomarcador. Aporta una señal consistente en niños, sí, pero también deja claro que medir no es lo mismo que saber exactamente qué hacer clínicamente con esa información. El valor está en poder traducir estos datos en una intervención clínica, pero todavía nos falta claridad.Robberecht, H., Verlaet, A.A.J., Breynaert, A., De Bruyne, T. y Hermans, N. (2020). Magnesium, Iron, Zinc, Copper and Selenium Status in Attention-Deficit/Hyperactivity Disorder (ADHD). Molecules, 25(19), 4440.
Notas: Esta revisión me gusta porque introduce una capa de complejidad muy necesaria. En lugar de asumir que “bajo en sangre” equivale automáticamente a “déficit clínico” o a “necesita suplemento”, recuerda que los biomarcadores minerales cuentan historias parciales y a veces contradictorias. En un campo tan proclive a simplificarse en redes, ese matiz vale mucho. La ciencia no es siempre fácil de simplificar a historias de Instagram…Lange, K.W., Hauser, J., Lange, K.M. et al. (2017). The Role of Nutritional Supplements in the Treatment of ADHD: What the Evidence Says. Current Psychiatry Reports, 19(2), 8.
Notas: Un artículo de revisión especialmente útil como mapa general, porque pone bastante orden en un terreno donde es fácil mezclar plausibilidad biológica con eficacia clínica probada. Su tono prudente sigue siendo muy vigente: algunos nutrientes pueden ayudar en contextos concretos, pero la evidencia dista mucho de sostener promesas amplias o soluciones fáciles.Hunter, C., Smith, C., Davies, E., Dyall, S.C. y Gow, R.V. (2025). A closer look at the role of nutrition in children and adults with ADHD and neurodivergence. Frontiers in Nutrition, 12, 1586925.
Notas: Este trabajo me parece interesante porque intenta abrir la conversación nutricional más allá del TDAH infantil puro y duro, incorporando también adultos y otras formas de neurodivergencia. Justamente por eso conviene leerlo como lo que es: una pieza preliminar, útil para generar preguntas y detectar patrones, pero no para sostener afirmaciones clínicas fuertes por sí sola. Desde luego, no es un artículo que nos sirva para crear un “protocolo nutricional para el TDAH”.Allahyari, P., Abbas Torki, S., Aminnezhad Kavkani, B., Mahmoudi, Z., Mousavi Hoseini, M. S., Moradi, M., Alami, F., Keshavarz Mohammadian, M., Bahoo Sele Bani, S., Abbasi Mobarakeh, K., Shafaei, H., Khoshdooz, S., Hajipour, A., Doaei, S., & Gholamalizadeh, M. (2024). A systematic review of the beneficial effects of prebiotics, probiotics, and synbiotics on ADHD. Neuropsychopharmacology reports, 44(2), 300–307. https://doi.org/10.1002/npr2.12437
Notas: Una revisión útil porque resume bien el momento actual del campo: hay señales prometedoras, pero todavía demasiado enmarañamiento en cepas, duración, edad y medidas de resultado como para hablar con excesiva seguridad. En otras palabras, interesante, sí; listo para simplificaciones comerciales, no.Gomes, A., Soares, A., Correia, C. G., Castelo-Branco, M., & Oliveira, G. (2025). The effectiveness of the gut microbiota modulation on ADHD in adults: A systematic review. Current Developmental Disorders Reports. Advance online publication. https://doi.org/10.1007/s40501-025-00358-9
Notas: Esta revisión me parece muy valiosa precisamente porque baja el volumen del entusiasmo. En adultos con TDAH, el campo sigue siendo tan pequeño que una revisión sistemática acaba trabajando con apenas tres ensayos aleatorizados. A veces, el dato más importante de una revisión no es lo que confirma, sino lo poco que todavía sabemos.Levy Schwartz, M., Magzal, F., Yehuda, I., & Tamir, S. (2024). Exploring the impact of probiotics on adult ADHD management through a double-blind RCT. Scientific reports, 14(1), 26830. https://doi.org/10.1038/s41598-024-73874-y
Notas: Me parece uno de los estudios más interesantes en adultos, no porque resuelva el tema, sino porque conecta síntomas de TDAH, síntomas gastrointestinales y rendimiento funcional dentro del mismo ensayo. También me gusta que encuentre una respuesta más favorable en participantes más jóvenes, porque sugiere que la historia quizá no vaya solo de “si funciona o no”, sino también de cuándo, en quién y bajo qué condiciones. Los matices son lo que más me fascina de la ciencia según se va desplegando en campos tan complejos como este.Lawrence, K., Myrissa, K., Toribio-Mateas, M., Minini, L., & Gregory, A. M. (2022). Trialling a microbiome-targeted dietary intervention in children with ADHD-the rationale and a non-randomised feasibility study. Pilot and feasibility studies, 8(1), 108. https://doi.org/10.1186/s40814-022-01058-4
Notas: Para mí, este estudio tiene valor porque cambia el foco desde el suplemento aislado hacia una intervención alimentaria dirigida a la microbiota. No intenta demostrar demasiado pronto una eficacia espectacular; hace algo más importante al principio de un programa de investigación: comprobar si el enfoque es viable, seguro y razonablemente habitable en la vida real. Además soy uno de los autores, y fue una experiencia enriquecedora trabajar en el diseño, la realización del estudio y la interpretación de los datos.Lawrence, K., Fibert, P., Hobbs, J., Myrissa, K., Toribio-Mateas, M. A., Quadt, F., Cotter, P. D., & Gregory, A. M. (2023). Randomised controlled trial of the effects of kefir on behaviour, sleep and the microbiome in children with ADHD: a study protocol. BMJ open, 13(12), e071063. https://doi.org/10.1136/bmjopen-2022-071063
Notas: Aunque sea un protocolo, me parece una referencia importante porque muestra ambición metodológica y claridad conceptual. Sitúa el kéfir no como un “probiótico natural” sin más, sino como una intervención alimentaria compleja, con potencial para influir en conducta, sueño y microbioma dentro de un diseño más riguroso. Igualmente soy uno de los autores y la razón por la que se publicó es muy importante. Aprendimos mucho en nuestro estudio preliminar, con lo cual necesitábamos ser transparentes con la comunidad científica y admitir que algunas de nuestras suposiciones no eran correctas, y que los métodos que habíamos utilizado en el estudio de factibilidad no eran los más adecuados.Lawrence, K., Fibert, P., Toribio-Mateas, M., Gregory, A. M., Hobbs, J., Quadt, F., Wright, S., Cotter, P. D., Patel, S., & Myrissa, K. (2025). Effects of kefir on symptoms, sleep, and gut microbiota in children with ADHD: a randomised controlled trial. BMC psychiatry, 25(1), 1117. https://doi.org/10.1186/s12888-025-07568-8
Notas: Este ensayo me parece especialmente valioso porque nos permitió llevar la conversación un paso más allá del “probiotic pill mindset” y estudiar un alimento fermentado completo en un ensayo controlado. Lo que más me interesa no es vender el kéfir como solución, sino abrir una vía más ecológica y más alimentaria para pensar la modulación del eje intestino-cerebro en TDAH. Estoy muy orgulloso del trabajo que mis compañeros y yo hicimos, y de haber podido publicarlo en una revista de psiquiatría tan eminente.Min, L., Ablitip, A., Wang, R., Luciana, T., Wei, M., & Ma, X. (2024). Effects of Exercise on Gut Microbiota of Adults: A Systematic Review and Meta-Analysis. Nutrients, 16(7), 1070. https://doi.org/10.3390/nu16071070
Notas: Esta revisión me parece útil porque refuerza una de las ideas centrales de este artículo: el movimiento no beneficia solo al músculo o al ánimo, también parece dialogar con la ecología intestinal. Tengo que ser honesto y decir que no convierte el ejercicio en una panacea, pero sí ayuda a pensar en el cuerpo como una red de sistemas con el potencial de influirse y beneficiarse entre ellos.Al-Beltagi, M., Saeed, N. K., Bediwy, A. S., El-Sawaf, Y., Elbatarny, A., & Elbeltagi, R. (2025). Exploring the gut-exercise link: A systematic review of gastrointestinal disorders in physical activity. World journal of gastroenterology, 31(22), 106835. https://doi.org/10.3748/wjg.v31.i22.106835
Notas: Me parece una revisión interesante porque amplía la conversación entre ejercicio e intestino más allá de la microbiota aislada y la sitúa dentro de una fisiología más global. En el contexto de este artículo, ayuda a sostener la idea de que moverse afecta mucho más que el gasto energético, modificando el terreno corporal desde el que vivimos el TDAH.







Te leo en comentarios
Comparte una idea, una reflexión o una pregunta.
Mantengamos este espacio amable y respetuoso, por favor. Gracias.